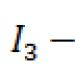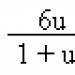Алюминий – элемент с порядковым номером 13, относительной атомной массой – 26,98154. Находится в III периоде, III группе, главной подгруппе. Электронная конфигурация: 1s 2 2s 2 2p 6 3s 2 3p 1 3d 0 . Устойчивая степень окисления алюминия – «+3». Образующийся при этом катион обладает оболочкой благородного газа, что способствует его устойчивости, но отношение заряда к радиусу, то есть концентрация заряда, достаточно высоки, что повышает энергию катиона. Эта особенность приводит к тому, что алюминий наряду с ионными соединениями образует целый ряд ковалентных соединений, а его катион подвергается в растворе значительному гидролизу.
Валентность I алюминий может проявлять только при температуре выше 1500 о С. Известны Al 2 O и AlCl.
По физическим свойствам алюминий – типичный металл, с высокой тепло- и электропроводностью, уступающий только серебру и меди. Потенциал ионизации алюминия не очень высок, поэтому от него можно было бы ожидать большой химической активности, но она значительно снижена из-за того, что на воздухе металл пассивируется за счет образования на его поверхности прочной оксидной пленки. Если металл активизировать: а) механически удалить пленку, б) амальгамировать (привести во взаимодействие с ртутью), в) использовать порошок, то такой металл становится настолько реакционноспособным, что взаимодействует даже с влагой и кислородом воздуха, разрушаясь при этом в соответствии с процессом:
4(Al,Hg) +3O 2 + 6H 2 O = 4Al(OH) 3 + (Hg)
Взаимодействие с простыми веществами.
1. Порошкообразный алюминий при сильном нагревании реагирует с кислородом. Эти условия нужны из-за пассивации, а сама реакция образования оксида алюминия сильно экзотермична – выделяется 1676 кДж/моль теплоты.
2. С хлором и бромом реагирует при стандартных условиях, способен даже загораться в их среде. Не реагирует только с фтором, т.к. фторид алюминия, подобно оксиду, образует на поверхности металла защитную солевую пленку. С иодом реагирует при нагревании и в присутствии воды как катализатора.
3. С серой реагирует при сплавлении, давая сульфид алюминия состава Al 2 S 3 .
4. C фосфором также реагирует при нагревании с образованием фосфида: AlP.
5. Непосредственно с водородом алюминий не взаимодействует.
6. С азотом взаимодействует при 800 о С, давая нитрид алюминия (AlN). Следует сказать, что горение алюминия на воздухе происходит примерно при таких температурах, поэтому продуктами горения (с учетом состава воздуха) являются одновременно и оксид, и нитрид.
7. С углеродом алюминий взаимодействует при еще более высокой температуре: 2000 о С. Карбид алюминия состава Al 4 C 3 относится к метанидам, в его составе нет связей С-С, и при гидролизе выделяется метан: Al 4 C 3 + 12H 2 O = 4Al(OH) 3 + 3CH 4
Взаимодействие со сложными веществами
1. С водой активированный (лишенный защитной пленки) алюминий активно взаимодействует с выделением водорода: 2Al (акт.) + 6H 2 O = 2Al(OH) 3 + 3H 2 Гидроксид алюминия получается в виде белого рыхлого порошка, отсутствие пленки не мешает прохождению реакции до конца.
2. Взаимодействие с кислотами: а) С кислотами-неокислителями алюминий активно взаимодействует в соответствии с уравнением: 2Al + 6H 3 O + + 6H 2 O = 2 3+ + 3H 2 ,
б) С кислотами-окислителями взаимодействие происходит со следующими особенностями. Концентрированные азотная и серная кислоты, а также очень разбавленная азотная кислота пассивируют алюминий (быстрое окисление поверхности приводит к образованию оксидной пленки) на холоду. При нагревании пленка нарушается, и реакция проходит, но из концентрированных кислот при нагревании выделяются только продукты их минимального восстановления: 2Al + 6H 2 SO 4 (конц) = Al 2 (SO 4) 3 + 3SO 2 6H 2 O Al + 6HNO 3 (конц) = Al(NO 3) 3 + 3NO 2 + 3H 2 O С умеренно разбавленной азотной кислотой в зависимости от условий реакции можно получить NO, N 2 O, N 2 , NH 4 + .
3. Взаимодействие со щелочами. Алюминий является амфотерным элементом (по химическим свойствам), т.к. обладает достаточно большой для металлов электроотрицательностью – 1,61. Поэтому он достаточно легко растворяется в растворах щелочей с образованием гидроксокомплексов и водорода. Состав гидроксокомплекса зависит от соотношения реагентов: 2Al + 2NaOH + 6H 2 O = 2Na + 3H 2 2Al + 6NaOH + 6H 2 O = 2Na 3 + 3H 2 Соотношение алюминия и водорода определяется электронным балансом происходящей между ними окислительно-восстановительной реакции и от соотношения реагентов не зависит.
4. Низкий потенциал ионизации и большое сродство к кислороду (большая устойчивость оксида) приводят к тому, что алюминий активно взаимодействует с оксидами многих металлов, восстанавливая их. Реакции проходят при начальном нагревании с дальнейшим выделением теплоты, так что температура повышается до 1200 о – 3000 о С. Смесь 75% алюминиевого порошка и 25% (по массе) Fe 3 O 4 называют «термитом». Раньше реакцию горения этой смеси использовали для сварки рельсов. Восстановление металлов из оксидов при помощи алюминия называется алюмотермией и используется в промышленности как способ получения таких металлов как марганец, хром, ванадий, вольфрам, ферросплавы.
5. С растворами солей алюминий взаимодействует двумя разными способами. 1. Если в результате гидролиза раствор соли имеет кислую или щелочную среду, происходит выделение водорода (с кислыми растворами реакция идет только при значительном нагревании, т.к. защитная оксидная пленка лучше растворяется в щелочах, чем в кислотах). 2Al + 6KHSO 4 + (H 2 O) = Al 2 (SO 4) 3 + 3K 2 SO 4 +3H 2 2Al + 2K 2 CO 3 + 8H 2 O = 2K + 2KHCO 3 + 3H 2 . 2. Алюминий может вытеснять из состава соли металлы, стоящие в ряду напряжения правее, чем он, т.е. фактически будет окисляться катионами этих металлов. Из-за оксидной пленки эта реакция проходит не всегда. Например, хлорид-анионы способны нарушать пленку, и реакция 2Al + 3FeCl 2 = 2AlCl 3 + 3Fe проходит, а аналогичная реакция с сульфатами при комнатной температуре не пойдет. С активированным алюминием любое взаимодействие, не противоречащее общему правилу, пойдет.
Соединения алюминия.
1. Оксид (Al 2 O 3). Известен в виде нескольких модификаций, большинство из которых очень прочны и химически инертны. Модификация α-Al 2 O 3 встречается в природе в виде минерала корунд. В кристаллической решетке этого соединения катионы алюминия иногда частично замещены на катионы других металлов, что придает минералу окраску. Примесь Cr(III) дает красный цвет, такой корунд – это уже драгоценный камень рубин. Примесь Ti(III) и Fe(III) дает сапфир синего цвета. Химически активна аморфная модификация. Оксид алюминия – типичный амфотерный оксид, реагирующий как с кислотами и кислотными оксидами, так и со щелочами и основными оксидами, причем со щелочами предпочтительнее. Продукты реакции в растворе и в твердой фазе при сплавлении отличаются: Na 2 O + Al 2 O 3 = 2NaAlO 2 (сплавление) – метаалюминат натрия, 6NaOH + Al 2 O 3 = 2Na 3 AlO 3 + 3H 2 O (сплавление) – ортоалюминат натрия, Al 2 O 3 + 3CrO 3 = Al 2 (CrO 4) 3 (сплавление) – хромат алюминия. Кроме оксидов и твердых щелочей алюминий при сплавлении реагирует с солями, образованными летучими кислотными оксидами, вытесняя их из состава соли: K 2 CO 3 + Al 2 O 3 = 2KAlO 2 + CO 2 Реакции в растворе: Al 2 O 3 + 6HCl = 2 3+ + 6Cl 1- + 3H 2 O Al 2 O 3 +2 NaOH + 3H 2 O =2 Na – тетрагидроксоалюминат натрия. Тетрагидроксоалюминат-анион на самом деле является тетрагидроксодиакваанионом 1- , т.к. координационное число 6 для алюминия предпочтительнее. При избытке щелочи образуется гексагидроксоалюминат: Al 2 O 3 + 6NaOH + 3H 2 O = 2Na 3 . Кроме кислот и щелочей можно ожидать реакций с кислыми солями: 6KHSO 4 + Al 2 O 3 = 3K 2 SO 4 + Al 2 (SO 4) 3 + 3H 2 O.
3. Гидроксиды алюминия . Известно два гидроксида алюминия – метагидроксид –AlO(OH) и ортогидроксид – Al(OH) 3 . Оба они в воде не растворяются, но также являются амфотерными, поэтому растворяются в растворах кислот и щелочей, а также солей, имеющих кислую или щелочную среду в результате гидролиза. При сплавлении гидроксиды реагируют аналогично оксиду. Как все нерастворимые основания гидроксиды алюминия при нагревании разлагаются: 2Al(OH) 3 = Al 2 O 3 + 3H 2 O. Растворяясь в щелочных растворах, гидроксиды алюминия не растворяются в водном аммиаке, поэтому их можно осадить аммиаком из растворимой соли: Al(NO 3) 3 + 3NH 3 + 2H 2 O = AlO(OH)↓ + 3NH 4 NO 3 , по этой реакции получается именно метагидроксид. Осадить гидроксид действием щелочей сложно, т.к. получившийся осадок легко растворяется, и суммарная реакция имеет вид: AlCl 3 +4 NaOH = Na + 3NaCl
4. Соли алюминия. Почти все соли алюминия хорошо растворимы в воде. Нерастворимы фосфат AlPO 4 и фторид AlF 3 . Т.к. катион алюминия имеет большую концентрацию заряда, его аквакомплекс приобретает свойства катионной кислоты: 3+ + H 2 O = H 3 O + + 2+ , т.е. соли алюминия подвергаются сильному гидролизу по катиону. В случае солей слабых кислот из-за взаимного усиления гидролиза по катиону и аниону гидролиз становится необратимым. В растворе полностью разлагаются водой или не могут быть получены по реакции обмена карбонат, сульфит, сульфид и силикат алюминия: Al 2 S 3 + 6H 2 O = 2Al(OH) 3 ↓ + 3H 2 S 2Al(NO 3) 3 + 3K 2 CO 3 + 3H 2 O = 2Al(OH) 3 ↓ + 3CO 2 + 6KNO 3 . Для некоторых солей гидролиз становится необратимым при нагревании. Влажный ацетат алюминия при нагревании разлагается в соответствии с уравнением: 2Al(OOCCH 3) 3 + 3H 2 O = Al 2 O 3 + 6CH 3 COOH В случае галогенидов алюминия разложению соли способствует уменьшение растворимости газообразных галогеноводородов при нагревании: AlCl 3 + 3H 2 O = Al(OH) 3 ↓ + 3HCl. Из галогенидов алюминия только фторид является ионным соединением, остальные галогениды – ковалентные соединения, их температуры плавления существенно ниже, чем у фторида, хлорид алюминия способен возгоняться. При очень высокой температуре в парах находятся одиночные молекулы галогенидов алюминия, имеющие плоское треугольное строение из-за sp 2 -гибридизации атомных орбиталей центрального атома. Основное состояние этих соединений в парах и в некоторых органических растворителях – это димеры, например, Al 2 Cl 6 . Галогениды алюминия являются сильными кислотами Льюиса, т.к. имеют вакантную атомную орбиталь. Растворение в воде, поэтому происходит с выделением большого количества теплоты. Интересным классом соединений алюминия (как и других трехвалентных металлов) являются квасцы – 12-водные двойные сульфаты M I M III (SO 4) 2 , которые при растворении как все двойные соли дают смесь соответствующих катионов и анионов.
5. Комплексные соединения. Рассмотрим гидроксокомплексы алюминия. Это соли, в которых комплексная частица является анионом. Все соли растворимые. Разрушаются при взаимодействии с кислотами. При этом сильные кислоты растворяют образующийся ортогидроксид, а слабые или соответствующие им кислотные оксиды (H 2 S, CO 2 , SO 2) его осаждают: K +4HCl = KCl + AlCl 3 + 4H 2 O K + CO 2 = Al(OH) 3 ↓ + KHCO 3
При прокаливании гидроксоалюминаты превращаются в орто - или метаалюминаты, теряя воду.
Железо
Элемент с порядковым номером 26, с относительной атомной массой 55,847. Относится к 3d-семейству элементов, имеет электронную конфигурацию: 3d 6 4s 2 и в периодической системе находится в IV периоде, VIII группе, побочной подгруппе. В соединениях железо преимущественно проявляет степени окисления +2 и +3. Ион Fe 3+ имеет наполовину заполненную d-электронную оболочку, 3d 5 , что придает ему дополнительную устойчивость. Значительно труднее достигаются степени окисления +4, +6, +8.
По физическим свойствам железо – серебристо-белый, блестящий, относительно мягкий, ковкий, легко намагничивающийся и размагничивающийся металл. Температура плавления 1539 о С. Имеет несколько аллотропных модификаций, отличающихся типом кристаллической решетки.
Свойства простого вещества.
1. При горении на воздухе образует смешанный оксид Fe 3 O 4 , а при взаимодействии с чистым кислородом – Fe 2 O 3 . Порошкообразное железо пирофорно – самовоспламеняется на воздухе.
2. Фтор, хлор и бром легко реагируют с железом, окисляя его до Fe 3+ . С иодом образуется FeJ 2 , так как трехвалентный катион железа окисляет иодид-анион, в связи с чем, соединения FeJ 3 не существует.
3. По аналогичной причине не существует соединения Fe 2 S 3 , а взаимодействие железа и серы при температуре плавления серы приводит к соединению FeS. При избытке серы получается пирит – дисульфид железа (II) – FeS 2 . Образуются также нестехиометрические соединения.
4. С остальными неметаллами железо реагирует при сильном нагревании, образуя твердые растворы или металлоподобные соединения. Можно привести реакцию, идущую при 500 о С: 3Fe + C = Fe 3 C. Такое соединение железа и углерода называется цементит.
5. Со многими металлами железо образует сплавы.
6. На воздухе при комнатной температуре железо покрыто оксидной пленкой, поэтому с водой не взаимодействует. Взаимодействие с перегретым паром дает следующие продукты: 3Fe + 4H 2 O (пар) = Fe 3 O 4 + 4H 2 . В присутствии кислорода железо взаимодействует даже с влагой воздуха: 4Fe + 3O 2 + 6H 2 O = 4Fe(OH) 3 . Приведенное уравнение отражает процесс ржавления, которому подвергается в год до 10% металлических изделий.
7. Так как железо стоит в ряду напряжения до водорода, оно легко реагирует с кислотами-неокислителями, но окисляется при этом только до Fe 2+ .
8. Концентрированные азотная и серная кислоты пассивируют железо, но при нагревании реакция происходит. Разбавленная азотная кислота реагирует и при комнатной температуре. Со всеми кислотами-окислителями железо дает соли железа (III) (по некоторым сведениям, с разбавленной азотной кислотой возможно образование нитрата железа (II)), а восстанавливает HNO 3 (разб.) до NO, N 2 O, N 2 , NH 4 + в зависимости от условий, а HNO 3 (конц.) – до NO 2 из-за нагревания, которое необходимо для прохождения реакции.
9. Железо способно реагировать с концентрированными (50%) щелочами при нагревании: Fe + 2KOH + 2H 2 O = K 2 + H 2
10. Реагируя с растворами солей менее активных металлов, железо вытеняет эти металлы из состава соли, превращаясь в двухвалентный катион: CuCl 2 + Fe = FeCl 2 + Cu.
Свойства соединений железа.
Fe 2+ Отношение заряда к радиусу данного катиона близко к таковому у Mg 2+ , поэтому химическое поведение оксида, гидроксида и солей двухвалентного железа подобно поведению соответствующих соединений магния. В водном растворе катион двухвалентного железа образует аквакомплекс 2+ бледно-зеленого цвета. Этот катион легко окисляется даже прямо в растворе кислородом воздуха. В растворе FeCl 2 содержатся комплексные частицы 0 . Концентрация заряда такого катиона невелика, поэтому гидролиз солей умеренный.
1. FeO - основной оксид, черного цвета, в воде не растворяется. Легко растворяется в кислотах. При нагревании свыше 500 0 С диспропорционирует: 4FeO = Fe + Fe 3 O 4 . Он может быть получен при осторожном прокаливании соответствующих гидроксида, карбоната и оксалата, тогда как термическое разложение других солей Fe 2+ приводит к образованию оксида трехвалентного железа: FeC 2 O 4 = FeO + CO + CO 2 , но 2 FeSO 4 = Fe 2 O 3 + SO 2 + SO 3 4Fe(NO 3) 2 = 2Fe 2 O 3 + 8NO 2 + O 2 Сам оксид железа (II) может выступать как окислитель, например, при нагревании идет реакция: 3FeO + 2NH 3 = 3Fe + N 2 +3H 2 O
2. Fe(OH) 2 – гидроксид железа (II) – нерастворимое основание. Реагирует с кислотами. С кислотами-окислителями происходит одновременно кислотно-основное взаимодействие и окисление до трехвалентного железа: 2Fe(OH) 2 + 4H 2 SO 4 (конц) = Fe 2 (SO 4) 3 + SO 2 + 4H 2 O. Может быть получен по обменной реакции из растворимой соли. Это соединение белого цвета, которое на воздухе сначала зеленеет из-за взаимодействия с влагой воздуха, а затем буреет из-за окисления кислородом воздуха: 4Fe(OH) 2 + 2H 2 O + O 2 = 4Fe(OH) 3 .
3. Соли. Как уже говорилось, большинство солей Fe(II) медленно окисляются на воздухе или в растворе. Наиболее устойчивой к окислению является соль Мора – двойной сульфат железа (II) и аммония: (NH 4) 2 Fe(SO 4) 2 . 6H 2 O. Катион Fe 2+ легко окисляется до Fe 3+ , поэтому большинство окислителей, в частности, кислоты-окислители окисляют соли двухвалентного железа. При обжиге сульфида и дисульфида железа получается оксид железа (III) и оксид серы (IV): 4FeS 2 + 11O 2 = 2Fe 2 O 3 + 8SO 2 Сульфид железа (II) растворяется также в сильных кислотах: FeS + 2HCl = FeCl 2 + 2H 2 S Карбонат железа (II) нерастворим, тогда как гидрокарбонат в воде растворяется.
Fe 3+ По отношению заряда к радиусу данный катион соответствует катиону алюминия, поэтому свойства соединений катиона железа (III) аналогичны соответствующим соединениям алюминия.
Fe 2 O 3 – гематит, амфотерный оксид, у которого преобладают основные свойства. Амфотерность проявляется в возможности сплавления с твердыми щелочами и карбонатами щелочных металлов: Fe 2 O 3 + 2NaOH = H 2 O + 2NaFeO 2 – желтого или красного цвета, Fe 2 O 3 + Na 2 CO 3 = 2NaFeO 2 + CO 2 . Ферраты (II) разлагаются водой с выделением Fe 2 O 3 . nH 2 O.
Fe 3 O 4 - магнетит, вещество черного цвета, которое можно рассматривать либо как смешанный оксид – FeO . Fe 2 O 3 , либо как оксометаферрат (III) железа (II): Fe(FeO 2) 2 . При взаимодействии с кислотами дает смесь солей: Fe 3 O 4 + 8HCl = FeCl 2 + 2FeCl 3 + 4H 2 O.
Fe(OH) 3 или FeO(OH) – красно-бурый студенистый осадок, амфотерный гидроксид. Кроме взаимодействий с кислотами реагирует с горячим концентрированным раствором щелочи и сплавляется с твердыми щелочами и карбонатами: Fe(OH) 3 + 3KOH = K 3 .
Соли. Большинство солей трехвалентного железа растворимо. Так же как соли алюминия, они подвергаются сильному гидролизу по катиону, который в присутствии анионов слабых и нестойких или нерастворимых кислот может стать необратимым: 2FeCl 3 + 3Na 2 CO 3 + 3H 2 O = 2Fe(OH) 3 + 3CO 2 + 6NaCl. При кипячении раствора хлорида железа (III) гидролиз также можно сделать необратимым, т.к. растворимость хлороводорода как любого газа при нагревании уменьшается и он уходит из сферы реакции: FeCl 3 + 3H 2 O = Fe(OH) 3 + 3HCl (при нагревании).
Окислительная способность данного катиона очень высока, особенно, по отношению к превращению в катион Fe 2+ : Fe 3+ + ē = Fe 2+ φ o =0,77в. В результате чего:
а) растворы солей трехвалентного железа окисляют все металлы вплоть до меди: 2Fe(NO 3) 3 + Cu = 2Fe(NO 3) 2 + Cu(NO 3) 2 ,
б) обменные реакции с солями, содержащими легко окисляемые анионы, проходят одновременно с их окислением: 2FeCl 3 + 2KJ = FeCl 2 + J 2 + 2KCl 2FeCl 3 + 3Na 2 S = 2FeS + S + 6NaCl
Как и другие трехвалентные катионы, железо (III) способно к образованию квасцов – двойных сульфатов с катионами щелочных металлов или аммония, например: NH 4 Fe(SO 4) 2 . 12H 2 O.
Комплексные соединения. Оба катиона железа склонны к образованию анионных комплексов, особенно железо (III). FeCl 3 + KCl = K, FeCl 3 + Cl 2 = Cl + - . Последняя реакция отражает действие хлорида железа (III) как катализатора электрофильного хлорирования. Интерес представляют цианидные комплексы: 6KCN + FeSO 4 = K 4 – гексацианоферрат (II) калия, желтая кровяная соль. 2K 4 + Cl 2 = 2K 3 + 2KCl – гексацианоферрат (III) калия, красная кровяная соль. Комплекс двухвалентного железа дает с солью трехвалентного железа синий осадок или раствор в зависимости от соотношения реагентов. Такая же реакция происходит между красной кровяной солью и любой солью двухвалентного железа. В первом случае осадок называли берлинской лазурью, во втором – турнбулевой синью. Позже выяснилось, что, по крайней мере, растворы имеют одинаковый состав: K – гексацианоферрат железа (II,III) калия. Описанные реакции являются качественными на наличие в растворе соответствующих катионов железа. Качественной реакцией на наличие катиона трехвалентного железа является появленме кроваво-красной окраски при взаимодействии с тиоцианатом (роданидом) калия:2FeCl 3 + 6KCNS = 6KCl + Fe.
Fe +6 . Степень окисления +6 для железа малоустойчива. Удается получить только анион FeO 4 2- , который существует только при pH>7-9, но при этом является сильным окислителем.
Fe 2 O 3 + 4KOH + 3KNO 3 = 2K 2 FeO 4 + 3KNO 2 + 2H 2 O
Fe (опилки) + H 2 O + KOH + KNO 3 = K 2 FeO 4 + KNO 2 + H 2
2Fe(OH) 3 + 3Cl 2 + 10KOH = 2K 2 FeO 4 + 6KCl + 6H 2 O
Fe 2 O 3 + KClO 3 + 4KOH = 2K 2 FeO 4 + KCl + 2H 2 O
4K 2 FeO 4 + 6H 2 O = 4FeO(OH)↓ + 8KOH + 3O 2
4BaFeO 4 (нагревание) = 4BaO + 2Fe 2 O 3 + 3O 2
2K 2 FeO 4 + 2CrCl 3 + 2HCl = FeCl 3 + K 2 Cr 2 O 7 + 2KCl + H 2 O
Получение железа в промышленности:
А) доменный процесс: Fe 2 O 3 + C = 2FeO + CO
FeO + C = Fe + CO
FeO + CO = Fe + CO 2
Б) алюмотермия: Fe 2 O 3 + Al = Al 2 O 3 + Fe
ХРОМ – элемент с порядковым номером 24, с относительной атомной массой 51,996. Относится к 3d-семейству элементов, имеет электронную конфигурацию 3d 5 4s 1 и в периодической системе находится в IV периоде, VI группе, побочной подгруппе. Возможные степени окисления: +1, +2, +3, +4, +5, +6. Из них наиболее устойчивыми являются +2, +3, +6, а минимальной энергией обладает +3.
По физическим свойствам хром – серовато-белый, блестящий, твердый металл с температурой плавления 1890 о С. Прочность его кристаллической решетки обусловлена наличием пяти неспаренных d-электронов, способных к частичному ковалентному связыванию.
Химические свойства простого вещества.
При низких температурах хром инертен из-за наличия оксидной пленки, не взаимодействует с водой и воздухом.
1. С кислородом взаимодействует при температурах выше 600 о С. При этом образуется оксид хрома (III) – Cr 2 O 3 .
2. Взаимодействие с галогенами происходит по-разному: Cr + 2F 2 = CrF 4 (при комнатной температуре), 2Cr + 3Cl 2 (Br 2) = 2CrCl 3 (Br 3), Cr + J 2 = CrJ 2 (при значительном нагревании). Следует сказать, что иодид хрома (III) может существовать и получается по обменной реакции в виде кристаллогидрата CrJ 3 . 9H 2 O, но его термическая устойчивость невелика, и при нагревании он разлагается на CrJ 2 и J 2 .
3. При температуре выше 120 о С хром взаимодействует с расплавленной серой, давая сульфид хрома (II) – CrS (черного цвета).
4. При температурах выше 1000 о С хром реагирует с азотом и углеродом, давая нестехиометрические, химически инертные соединения. Среди них можно отметить карбид с примерным составом CrC, который по твердости приближается к алмазу.
5. С водородом хром не реагирует.
6. Реакция с водяным паром проходит следующим образом: 2Cr + 3H 2 O = Cr 2 O 3 + 3H 2
7. Реакция с кислотами-неокислителями происходит достаточно легко, при этом образуется аква-комплекс 2+ небесно-голубого цвета, который устойчив только в отсутствие воздуха или в атмосфере водорода. В присутствии кислорода реакция идет иначе: 4Cr + 12HCl + 3O 2 = 4CrCl 3 + 6H 2 O. Разбавленные кислоты, насыщенные кислородом, даже пассивируют хром за счет образования на поверхности прочной оксидной пленки.
8. Кислоты- окислители: азотная кислота любой концентрации, серная концентрированная, хлорная кислота пассивируют хром так, что после обработки поверхности этими кислотами он уже не реагирует и с другими кислотами. Пассивация снимается при нагревании. При этом получаются соли хрома (III) и диоксиды серы или азота (из хлорной кислоты – хлорид). Пассивация за счет образования солевой пленки происходит при взаимодействии хрома с фосфорной кислотой.
9. Непосредственно со щелочью хром не реагирует, но вступает в реакцию со щелочными расплавами с добавлением окислителей: 2Cr + 2Na 2 CO 3 (ж) + 3O 2 = 2Na 2 CrO 4 + 2CO 2
10. Хром способен реагировать с растворами солей, вытесняя менее активные металлы (стоящие правее него в ряду напряжения) из состава соли. Сам хром при этом превращается в катион Cr 2+ .
Этот легкий металл с серебристо-белым оттенком в современной жизни встречается почти повсеместно. Физические и химические свойства алюминия позволяют широко использовать его в промышленности. Самые известные месторождения - в Африке, Южной Америке, в Карибском регионе. В России места добычи бокситов имеются на Урале. Мировыми лидерами по производству алюминия являются Китай, РФ, Канада, США.
Добыча Al
В природе этот серебристый металл в силу своей высокой химической активности встречается лишь в виде соединений. Наиболее известные геологические породы, содержащие алюминий, - это бокситы, глиноземы, корунды, полевые шпаты. Промышленное значение имеют бокситы и глиноземы, именно месторождения этих руд позволяют добывать алюминий в чистом виде.
Свойства
Физические свойства алюминия позволяют легко вытягивать заготовки этого металла в проволоку и прокатывать в тонкие листы. Этот металл не является прочным, для повышения данного показателя при выплавке его легируют различными добавками: медью, кремнием, магнием, марганцем, цинком. Для промышленного назначения важно еще одно физическое свойство вещества алюминия - это его способность быстро окисляться на воздухе. Поверхность изделия из алюминия в естественных условиях обычно покрыта тонкой оксидной пленкой, которая эффективно защищает металл и препятствует его коррозии. При уничтожении этой пленки серебристый металл быстро окисляется, при этом его температура заметно повышается.
Внутреннее строение алюминия
Физические и химические свойства алюминия во многом зависят от его внутреннего строения. Кристаллическая решетка этого элемента является разновидностью гранецентрированного куба.

Данный тип решетки присущ многим металлам, таким, как медь, бром, серебро, золото, кобальт и другие. Высокая теплопроводность и способность проводить электричество сделали этот металл одним из самых востребованных в мире. Остальные физические свойства алюминия, таблица которых представлена ниже, раскрывают полностью его свойства и показывают сферы их применения.

Легирование алюминия
Физические свойства меди и алюминия таковы, что при добавлении к алюминиевому сплаву некоторого количества меди его кристаллическая решетка искривляется, и прочность самого сплава повышается. На этом свойстве Al основано легирование легких сплавов для повышения их прочности и стойкости к воздействию агрессивной среды.
Объяснение процесса упрочнения лежит в поведении атомов меди в кристаллической решетке алюминия. Частицы Cu стремятся выпасть из кристаллической решетки Al, группируются на ее особых участках.

Там, где атомы меди образуют скопления, образуется кристаллическая решетка смешанного типа CuAl 2 , в которой частицы серебристого металла одновременно входят в состав и общей кристаллической решетки алюминия, и в состав решетки смешанного типа CuAl 2. Силы внутренних связей в искаженной решетке гораздо больше, чем в обычной. А значит, и прочность новообразованного вещества гораздо выше.
Химические свойства
Известно взаимодействие алюминия с разбавленными серной и соляной кислотой. При нагревании этот металл в них легко растворяется. Холодная концентрированная или сильно разбавленная азотная кислота не растворяет этот элемент. Водные растворы щелочей активно воздействуют на вещество, в процессе реакции образуя алюминаты - соли, в составе которых имеются ионы алюминия. Например:
Al 2 O 3 +3H2O+2NaOH=2Na
Получившееся в результате реакции соединение носит название тетрагидроксоалюминат натрия.
Тонкая пленка на поверхности алюминиевых изделий защищает этот металл не только от воздуха, но и от воды. Если эту тонкую преграду убрать, элемент станет бурно взаимодействовать с водой, выделяя из нее водород.
2AL+6H 2 O= 2 AL (OH) 3 +3Н 2
Образовавшееся вещество называется гидроксидом алюминия.
AL (OH) 3 реагирует с щелочью, образуя кристаллы гидроксоалюмината:
Al(OH) 2 +NaOH=2Na
Если это химическое уравнение сложить с предыдущим, получим формулу растворения элемента в щелочном растворе.
Al(OH) 3 +2NaOH+6H 2 O=2Na +3H 2
Горение алюминия
Физические свойства алюминия позволяют ему вступать в реакцию с кислородом. Если порошок этого металла или алюминиевую фольгу нагреть, то она вспыхивает и горит белым ослепительным пламенем. В конце реакции образуется оксид алюминия Al 2 O 3.
Глинозем
Полученный оксид алюминия имеет геологическое название глинозем. В естественных условиях он встречается в виде корунда - твердых прозрачных кристаллов. Корунд отличается высокой твердостью, в шкале твердых веществ его показатель составляет 9. Сам корунд бесцветен, но различные примеси могут окрасить его в красный и синий цвет, так получаются драгоценные камни, которые в ювелирном деле называются рубинами и сапфирами.
Физические свойства оксида алюминия позволяют выращивать эти драгоценные камни в искусственных условиях. Технические драгоценные камни используются не только для ювелирных украшений, они применяются в точном приборостроении, для изготовления часов и прочего. Широко используются искусственные кристаллы рубина и в лазерных устройствах.

Мелкозернистая разновидность корунда с большим количеством примесей, нанесенная на специальную поверхность, известна всем как наждак. Физические свойства оксида алюминия объясняют высокие абразивные свойства корунда, а также его твердость и устойчивость к трению.
Гидроксид алюминия
Al 2 (OH) 3 является типичным амфотерным гидроксидом. В соединении с кислотой это вещество образует соль, содержащую положительно заряженные ионы алюминия, в щелочах образует алюминаты. Амфотерность вещества проявляется в том, что он может вести себя и как кислота, и как щелочь. Это соединение может существовать и в желеобразном, и в твердом виде.

В воде практически не растворяется, но вступает в реакцию с большинством активных кислот и щелочей. Физические свойства гидроксида алюминия используются в медицине, это популярное и безопасное средство снижения кислотности в организме, его применяют при гастритах, дуоденитах, язвах. В промышленности Al 2 (OH) 3 используется в качестве адсорбента, он прекрасно очищает воду и осаждает растворенные в ней вредные элементы.
Промышленное использование
Алюминий был открыт в 1825 году. Поначалу данный металл ценился выше золота и серебра. Это объяснялось сложностью его извлечения из руды. Физические свойства алюминия и его способность быстро образовывать защитную пленку на своей поверхности затрудняли исследование этого элемента. Лишь в конце 19 века был открыт удобный способ плавки чистого элемента, пригодный для использования в промышленных масштабах.

Легкость и способность сопротивляться коррозии - уникальные физические свойства алюминия. Сплавы этого серебристого металла применяются в ракетной технике, в авто-, судо-, авиа- и приборостроении, в производстве столовых приборов и посуды.
Как чистый металл Al используется при изготовлении деталей для химической аппаратуры, электропроводов и конденсаторов. Физические свойства алюминия таковы, что его электропроводность не так высока, как у меди, но этот недостаток компенсируется легкостью рассматриваемого металла, что позволяет делать провода из алюминия более толстыми. Так, при одинаковой электропроводности алюминиевый провод весит в два раза меньше медного.
Не менее важным является применение Al в процессе алитирования. Так называется реакция насыщения поверхности чугунного или стального изделия алюминием с целью защиты основного металла от коррозии при нагревании.
В настоящее время изведанные запасы алюминиевых руд вполне сопоставимы с потребностями людей в этом серебристом металле. Физические свойства алюминия могут преподнести еще немало сюрпризов его исследователям, а сферы применения этого металла гораздо шире, чем можно представить.
ЧТО ТАКОЕ АЛЮМИНИЙ
Лёгкий, прочный, стойкий к коррозии и функциональный – именно это сочетание качеств сделало алюминий главным конструкционным материалом нашего времени. Алюминий есть в домах, в которых мы живем, автомобилях, поездах и самолетах, на которых мы преодолеваем расстояния, в мобильных телефонах и компьютерах, на полках холодильников и в современных интерьерах. А ведь еще 200 лет назад об этом металле мало что было известно.
«То, что казалось несбыточным на протяжении веков, что вчера было лишь дерзновенной мечтой, сегодня становится реальной задачей, а завтра - свершением».
Сергей Павлович Королев
учёный, конструктор, основоположник практической космонавтики
Алюминий – серебристо-белый металл, 13-й элемент периодической таблицы Менделеева. Невероятно, но факт: алюминий – самый распространенный металл на Земле, на него приходится более 8% всей массы земной коры, и это третий по распространенности химический элемент на нашей планете после кислорода и кремния.
При этом алюминий не встречается в природе в чистом виде из-за своей высокой химической активности. Вот почему мы узнали о нем относительно недавно. Формально алюминий был получен лишь в 1824 году, и прошло еще полвека, прежде чем началось его промышленное производство.
Чаще всего в природе алюминий встречается в составе квасцов . Это минералы, объединяющие в себе две соли серной кислоты: одну на основе щелочного металла (лития, натрия, калия, рубидия или цезия), а другую – на основе металла третьей группы таблицы Менделеева, преимущественно алюминия.
Квасцы и сегодня применяют при очистке воды, в кулинарии, медицине, косметологии, в химической и других отраслях промышленности. Кстати, свое имя алюминий получил как раз благодаря квасцам, которые на латыни назывались alumen.

Корунд
Рубины, сапфиры, изумруды и аквамарин являются минералами алюминия.
Первые два относятся к корундам – это оксид алюминия (Al 2 O 3) в кристаллической форме. Он обладает природной прозрачностью, а по прочности уступает только алмазам. Пуленепробиваемые стекла, иллюминаторы в самолетах, экраны смартфонов производятся именно с применением сапфира.
А один из менее ценных минералов корунда – наждак используется как абразивный материал, в том числе для создания наждачной бумаги.

На сегодняшний день известно почти 300 различных соединений и минералов алюминия – от полевого шпата, являющегося основным породообразующим минералом на Земле, до рубина, сапфира или изумруда, уже не столь распространенных.

Ханс Кристиан Эрстед (1777–1851) – датский физик, почетный член Петербургской академии наук (1830). Родился в городе Рудкёрбинге в семье аптекаря. В 1797 году окончил Копенгагенский университет, в 1806 – стал профессором.
Но каким бы распространенным ни был алюминий, его открытие стало возможным только, когда в распоряжении ученых появился новый инструмент, позволяющий расщеплять сложные вещества на простые, – электрический ток .
И в 1824 году с помощью процесса электролиза датский физик Ханс Кристиан Эрстед получил алюминий. Он был загрязнен примесями калия и ртути, задействованных в химических реакциях, однако это был первый случай получения алюминия.
Используя электролиз, алюминий производят и в наши дни.
Сырьем для производства алюминия сегодня служит еще одна распространенная в природе алюминиевая руда – бокситы
. Это глинистая горная порода, состоящая из разнообразных модификаций гидроксида алюминия с примесью оксидов железа, кремния, титана, серы, галлия, хрома, ванадия, карбонатных солей кальция, железа и магния – чуть ли не половины таблицы Менделеева. В среднем из 4-5 тонн бокситов производится 1 тонна алюминия.
Бокситы
Бокситы в 1821 году открыл геолог Пьер Бертье на юге Франции. Порода получила свое название в честь местности Ле-Бо (Les Baux), где была найдена. Около 90% мировых запасов бокситов сосредоточено в странах тропического и субтропического поясов – в Гвинее, Австралии, Вьетнаме, Бразилии, Индии и на Ямайке.

Из бокситов получают глинозем . Это оксид алюминия Al 2 O 3 , который имеет форму белого порошка и из которого путем электролиза на алюминиевых заводах производят металл.
Производство алюминия требует огромного количества электроэнергии. Для производства одной тонны металла необходимо около 15 МВт*ч энергии – столько потребляет 100-квартирный дом в течение целого месяца.Поэтому разумнее всего строить алюминиевые заводы поблизости от мощных и возобновляемых источников энергии. Самое оптимальное решение – гидроэлектростанции , представляющие самый мощный из всех видов «зеленой энергетики».
Свойства алюминия
Алюминий имеет редкое сочетание ценных свойств. Это один из самых легких металлов в природе: он почти в три раза легче железа, но при этом прочен, чрезвычайно пластичен и не подвержен коррозии, так как его поверхность всегда покрыта тончайшей, но очень прочной оксидной пленкой. Он не магнитится, отлично проводит электрический ток и образует сплавы практически со всеми металлами.

Легкий
В три раза легче железа

Прочный
Сравним по прочности со сталью

Пластичный
Поддается всем видам механической обработки

Нет коррозии
Тонкая оксидная пленка защищает от коррозии
Алюминий легко обрабатывается давлением, причем как в горячем, так и в холодном состоянии. Он поддается прокатке, волочению, штамповке. Алюминий не горит, не требует специальной окраски и не токсичен в отличие от пластика.
Очень высока ковкость алюминия: из него можно изготовить листы толщиной всего 4 микрона и тончайшую проволоку. А сверхтонкая алюминиевая фольга втрое тоньше человеческого волоса. Кроме того, по сравнению с другими металлами и материалами он более экономичен.
Высокая способность к образованию соединений с различными химическими элементами породила множество сплавов алюминия. Даже незначительная доля примесей существенно меняет характеристики металла и открывает новые сферы для его применения. Например, сочетание алюминия с кремнием и магнием в повседневной жизни можно встретить буквально на дороге – в форме литых колесных дисков, двигателей, в элементах шасси и других частей современного автомобиля. А если добавить в алюминиевый сплав цинк, то, возможно, вы сейчас держите его в руках, ведь именно этот сплав используется при производстве корпусов мобильных телефонов и планшетов. Тем временем ученые продолжают изобретать новые и новые алюминиевые сплавы.
Запасы алюминия
Около 75% алюминия, выпущенного за все время существования отрасли, используется до сих пор.
В статье использованы фотоматериалы © Shutterstock и © Rusal.
Алюминия оксид (глинозем) А1 2 О 3 , бесцв. кристаллы ; т. пл. 2044°С; т. кип. 3530 °С. Единственная стабильная до 2044°С кристаллич. модификация алюминия оксида-А1 2 О 3 (корунд ): решетка ромбоэдрич., а = 0,512 нм,= 55,25° (для гексагон. установки а = 0,475 нм, с = 1,299 нм, пространств. группа D 6 3d , z = 2); плотн. 3,99 г/см 3 ;Н° пл 111,4 кДж/моль ; ур-ния температурной зависимости: теплоемкости С° р = = 114,4 + 12,9*10 -3 Т - 34,3*10 5 Т 2 ДжДмоль*К) (298Т 1800 К), давления пара Igp (Па) = -54800/7+1,68 (до ~ 3500 К); температурный коэф. линейного расширения (7,2-8,6)*10 -6 К -1 (300Т1200 К); теплопроводность спеченного при 730°С образца 0,35 Вт/(моль*К); твердость по Моосу 9; показатель преломления для обыкновенного луча n 0 1,765, для необыкновенного п е 1,759.
Оксид алюминия (Al2O3) обладает исключительным набором свойств, таких как:
- Высокая твердость
- Хорошая теплопроводность
- Отличная коррозионная стойкость
- Низкая плотность
- Сохранение прочности в широком диапазоне температур
- Электроизоляционные свойства
- Невысокая стоимость относительно других керамических материалов
Все эти сочетания делают материал не заменимым при изготовлении коррозионностойких, износостойких, электроизоляционных и термостойких изделий для самых различных отраслей промышленности.
Основные области применения:
- Футеровка мельниц, гидроциклонов, бетономешалок, экструдеров, транспортеров, труб и прочего изнашиваемого оборудования
- Кольца торцовых уплотнений
- Фильеры, проводки, направляющие
- Подшипники скольжения, валы и футеровка проточных частей химических насосов
- Мелящие тела
- Части бумагоделательного оборудования
- Горелки
- Насадки экструдеров (керны)
- Тигли
- Элементы клапанов и запорной арматуры
- Сопла для аппаратов аргонно-дуговой сварки
- Электроизоляторы
Существует несколько модификаций оксида алюминия в зависимости от содержания основной фазы и примесей, которые отличаются прочностью и химической стойкостью
Гидроксид алюминия
Гидроксид алюминия Al(OH) 3 – бесцветное твердое вещество, нерастворимое в воде, входит в состав многих бокситов. Существует в четырех полиморфных модификациях. На холоде образуется α-Al(OH) 3 – байерит, а при осаждении из горячего раствора γ-Al(OH) 3 – гиббсит (гидаргилит), обе кристаллизуются в моноклинной сингонии, имеют слоистое строение, слои состоят из октаэдров , между слоями действует водородная связь. Существует также триклинный гиббсит γ’-Al(OH) 3 , триклинный нордстрандит β-Al(OH) 3 и две модификации оксогидроксида AlOOH – орторомбические бемит и диаспор. Аморфный гидроксид алюминия имеет переменный состав Al 2 O 3 · nH 2 O. При нагревании выше 180°С разлагается.
Химические свойства
Гидроксид алюминия – типичное амфотерное соединение, свежеполученный гидроксид растворяется в кислотах и щелочах:
2Al(OH) 3 + 6HCl = 2AlCl 3 + 6H 2 O
Al(OH) 3 + NaOH + 2H 2 O = Na.
При нагревании разлагается, процесс дегидратации довольно сложен и схематично может быть представлен следующим образом:
Al(OH) 3 = AlOOH + H 2 O;
2AlOOH = Al 2 O 3 + H 2 O.
Гидроксид алюминия - химическое вещество, которое представляет собой соединение оксида алюминия с водой. Может пребывать в жидком и твердом состояниях. Жидкий гидроксид является желеподобным прозрачным веществом, которое очень плохо растворяется в воде. Твердый гидроксид представляет собой кристаллическое вещество белого цвета, которое обладает пассивными химическими свойствами и не реагирует практически ни с одним другим элементом или соединением.
Хлорид алюминия
При обычном давлении возгоняется при 183 °C (под давлением плавится при 192,6 °C). В воде хорошо растворим (44,38 г в 100 г H 2 O при 25 °C); вследствие гидролиза дымит во влажном воздухе, выделяя HCl. Из водных растворов выпадает кристаллогидрат AlCl 3 · 6H 2 O - желтовато-белые расплывающиеся кристаллы. Хорошо растворим во многих органических соединениях (в этаноле - 100 г в 100 г спирта при 25 °C, в ацетоне, дихлорэтане , этиленгликоле, нитробензоле, тетрахлоруглероде и др.); однако практически не растворяется в бензоле и толуоле.
Сульфат алюминия
Сульфат алюминия - это соль белого цвета с серым, голубым или розовым оттенком, при обычных условиях существует в виде кристаллогидрата Al 2 (SO 4) 3 ·18H 2 O - бесцветных кристаллов. При нагревании теряет воду не плавясь, при прокаливании распадается на Al 2 O 3 и SO 3 и O 2 . Хорошо растворяется в воде. Технический сульфат алюминия можно получить, обрабатывая серной кислотой боксит или глину, а чистый продукт, - растворяя Al(OH) 3 в горячей концентрированной H 2 SO 4 .
Сульфат алюминия применяется как коагулянт для очистки воды хозяйственно-питьевого и промышленного назначения и для использования в бумажной, текстильной, кожевенной и других отраслях промышленности.
Используется в качестве пищевой добавки E-520
Карбид алюминия
Карбид алюминия получается прямой реакцией алюминия с углеродом в дуговой печи.
4 A l + 3 C ⟶ A l 4 C 3 {\displaystyle {\mathsf {4Al+3C\longrightarrow Al_{4}C_ Небольшое количество карбида алюминия является нормой в примеси технического карбида кальция. В электролитическом производстве алюминия данное соединение получается как продукт коррозии в графитовых электродах. Получается при реакции углерода с оксидом алюминия:Железо с алюминием
Ални - группа магнитотвёрдых (высококоэрцитивных) сплавов железо (Fe) - никель (Ni) - алюминий (Al).
Легирование ални-сплавов улучшает их магнитные характеристики, применяется легирование медью (например, сплав 24 % никеля, 4 % меди, 13 % алюминия и 59 % железа), кобальтом (сплавы альнико и магнико ). Примесь углерода снижает магнитные свойства сплава, его содержание не должно превышать 0,03 %.
Ални-сплавы характеризуются высокой твёрдостью и хрупкостью, поэтому для изготовления постоянных магнитов из них применяется литьё.
Алюминат натрия
Алюминат натрия - неорганическое соединение, сложный окисел натрия и алюминия с формулой NaAlO 2 , белое аморфное вещество, реагирует с водой.
Ортоалюминиевая кислота
Алюмина"ты, соли алюминиевых кислот: ортоалюминиевой H3 AlO3 , метаалюминиевой HAlO2 и др. В природе наиболее распространены Алюминаты общей формулы R, где R - Mg, Са, Be, Zn и др. Среди них различают: 1) октаэдрические разновидности, т. н. шпинели - Mg (благородная шпинель), Zn (ганитовая или цинковая шпинель) и др. и 2) ромбические разновидности - Be (хризоберилл) и др. (в формулах минералов атомы, составляющие структурную группу, обычно заключают в квадратные скобки).
Алюминаты щелочных металлов получают при взаимодействии Al или Al(OH)3 с едкими щелочами: Al(OH)3 + KOH = KAlO2 + 2H2 O. Из них а люминаты натрия NaAlO2, образующийся при щелочном процессе получения глинозёма, применяют в текстильном производстве как протраву. Алюминаты щёлочноземельных металлов получают сплавлением их окислов с Al2 O3 ; из них алюминаты кальция CaAl2 O4 служит главной составной частью быстро твердеющего глинозёмистого цемента.
Практическое значение приобрели Алюминаты редкоземельных элементов. Их получают совместным растворением окислов редкоземельных элементов R2 03 и Al(NO3 )3 в азотной кислоте, выпариванием полученного раствора до кристаллизации солей и прокаливанием последних при 1000-1100°С. Образование Алюминаты контролируется рентгеноструктурным, а также химическим фазовым анализом. Последний основан на различной растворимости исходных окислов и образуемого соединения (А., например, устойчивы в уксусной кислоте, в то время как окислы редкоземельных элементов хорошо растворяются в ней). Алюминаты редкоземельных элементов обладают большой химической стойкостью, зависящей от температур их предварительного обжига; в воде устойчивы при высоких температурах (до 350°С) под давлением. Наилучший растворитель Алюминаты редкоземельных элементов - соляная кислота. Алюминаты редкоземельных элементов отличаются высокой тугоплавкостью и характерной окраской. Их плотности составляют от 6500 до 7500 кг /м3 .
Алюминий-серебристо-белый металл, обладающий высокой электропроводностью и теплопроводностью. (Теплопроводность алюминия в 1,8 раз больше, чем у меди, и в 9 раз больше, чем у нержавеющей стали.) Он имеет невысокую плотность - приблизительно втрое меньше, чем у железа, меди и цинка. И все же это очень прочный металл.
Три электрона из внешней оболочки атома алюминия делокализованы по кристаллической решетке металлического алюминия. Эта решетка имеет грансцентрированную кубическую структуру, подобную решетке олова и золота (см. разд. 3.2). Поэтому алюминий обладает хорошей ковкостью.
Химические свойства
Алюминий образует соединения ионного и ковалентного типа. Он характеризуется высокой энергией ионизации (табл. 15.1). Плотность заряда (отношение заряда к радиусу) для иона очень велика по сравнению с катионами других металлов того же периода (см. табл. 15.2).

Рис. 15.2. Гидратированный ион алюминия.
Таблица 15.2. Отношение заряда к радиусу катионов

Поскольку ион имеет высокую плотность заряда, он обладает большой поляризующей способностью. Этим объясняется то, что изолированный ион обнаруживается лишь в очень немногих соединениях, например в безводном фториде алюминия и оксиде алюминия, причем даже эти соединения обнаруживают заметный ковалентный характер. В водном растворе ион поляризует молекулы воды, которые вследствие этого гидратируют катион (см. рис. 15.2). Эта гидратация характеризуется большой экзотермичностью:
Стандартный окислительно-восстановительный потенциал алюминия равен - 1,66 В:
Поэтому в электрохимическом ряду элементов алюминий расположен довольно высоко (см. разд. 10.5). Это заставляет предположить, что алюминий должен легко реагировать с кислородом и разбавленными минеральными кислотами. Однако, когда алюминий реагирует с кислородом, на его поверхности образуется тонкий непористый слой оксида. Этот слой предохраняет алюминий от дальнейшего взаимодействия с окружающей средой. Оксидный слой можно удалить с поверхности алюминия, натирая ее ртутью. После этого алюминий способен соединяться непосредственно с кислородом и другими неметаллами, например серой и азотом. Взаимодействие с кислородом приводит к реакции
Анодирование. Алюминий и легкие алюминиевые сплавы можно защитить еще больше, сделав толще естественный оксидный слой при помощи процесса, который называется анодированием. В этом процессе алюминиевый предмет помещают в качестве анода в электролизер, где в качестве электролита используется хромовая кислота либо серная кислота.
Алюминий реагирует с горячими разбавленными соляной и серной кислотами, образуя водород:
Сначала эта реакция протекает медленно из-за наличия оксидного слоя. Однако по мере того, как он удаляется, реакция становится все более интенсивной.
Концентрированная и разбавленная азотная кислота, а также концентрированная серная кислота делают алюминий пассивным. Это означает, что он не реагирует с указанными кислотами. Такая пассивность объясняется образованием тонкого слоя оксида на поверхности алюминия.
Растворы гидроксида натрия и других щелочей взаимодействуют с алюминием, образуя тетрагидроксоалюминат(III)-ионы и водород:
Если оксидный слой удален с поверхности, алюминий может выступать в роли восстановителя в окислительно-восстановительных реакциях (см. разд. 10.2). Он вытесняет металлы, расположенные ниже его в электрохимическом ряду, из их растворов. Например
Наглядным примером восстановительной способности алюминия является алюмотермитная реакция. Так называется реакция между порошкообразным алюминием и
оксидом В лабораторных условиях ее обычно инициируют, используя в качестве запала ленточку магния. Эта реакция протекает очень бурно, и в ней выделяется такое количество энергии, которого достаточно, чтобы расплавить образующееся железо:
Алюмотермитную реакцию используют для проведения алюмотермитной сварки; например, таким способом соединяют рельсы.
Оксид алюминия Оксид алюминия, или, как его часто называют, глинозем, представляет собой соединение, которое обладает как ионными, так и ковалентными свойствами. Он имеет температуру плавления и в расплавленном состоянии представляет собой электролит. По этой причине его часто считают ионным соединением. Однако в твердом состоянии оксид алюминия имеет каркасную кристаллическую структуру.
Корунд. Безводные формы оксида алюминия образуют в природных условиях минералы группы корундов. Корунд-это очень твердая кристаллическая форма оксида алюминия. Он используется в качестве абразивного материала, так как по твердости уступает только алмазу. Крупные и прозрачные, нередко окрашенные, кристаллы корундов ценятся как драгоценные камни. Чистый корунд бесцветен, однако наличие в нем небольшого количества примесей оксидов -металлов придает драгоценным корундам характерную окраску. Например, окраска рубина обусловлена наличием в корунде ионов а окраска сапфиров - наличием ионов кобальта Фиолетовая окраска аметиста обусловлена наличием в нем примеси марганца. Сплавляя глинозем с оксидами различных -металлов, можно получать искусственные драгоценные камни (см. также табл. 14.6 и 14.7).
Оксид алюминия нерастворим в воде и обладает амфотерными свойствами, вступая в реакцию как с разбавленными кислотами, так и с разбавленными щелочами. Реакция с кислотами описывается общим уравнением:
Реакция со щелочами приводит к образованию -иона:
Галогениды алюминия. Строение и химическая связь в галогенидах алюминия описаны в разд. 16.2.
Хлорид алюминия можно получать, пропуская сухой хлор либо сухой хлороводород над нагретым алюминием. Например
За исключением фторида алюминия, все остальные галогениды алюминия гидролизуются водой:
По этой причине галогениды алюминия в контакте с влажным воздухом «дымят».
Ионы алюминия. Мы уже указывали выше, что ион гидратируется в воде. При растворении солей алюминия в воде устанавливается следующее равновесие:
В этой реакции вода выступает в роли основания, так как она акцептирует протон, а гидратированный ион алюминия выступает в роли кислоты, так как он донирует протон. По этой причине соли алюминия обладают кислотными свойствами. Если в